Produits médicinaux GM: Cadre réglementaire
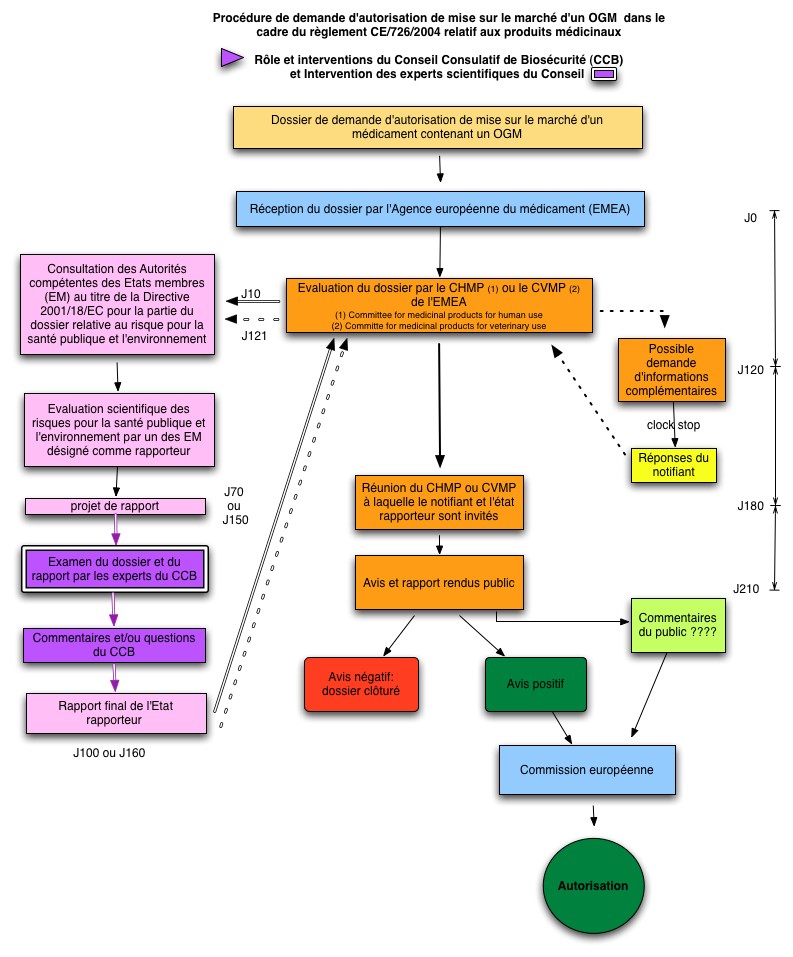
Le rôle et les interventions du Conseil dans les procédures réglementaires qui s'appliquent aux dossiers relatifs aux produits médicinaux soumis dans le cadre du Règlement (CE) 726/2004 sont résumés dans le diagramme figurant à droite du texte.
Pour l'évaluation scientifique de ces dossiers et en plus des dispositions du Règlement susmentionné, le Conseil peut se référer à plusieurs lignes directrices, énumérées sur le Belgian Biosafety Server.